销售服务热线
0574-62101882
编者按:
本文由基因港科学家张天佐编译。神经性疾病给人们带来了许多的麻烦,在日常生活中,“神经病”这个标签也常常被当做玩笑话用在身边朋友们的身上。但是对于真正患有“神经病”的患者来说,罹患该疾病是十分痛苦的体验。本文从多方位来解读NMN对于“痴线”(精神病)的帮助,通过试验再次证明了NMN对人体健康层面的益处。
2022年3月9日,浙江大学、暨南大学、复旦大学及协和医学院在自然杂志副刊发表了一篇文章。

文章标题很长很学术,直译来说就是〝SIRT2在OPC衰老时重新入核能够促进再髓鞘化〞。SIRT2指的是长寿蛋白“七贤者”中的老二,OPC指的是中枢神经中的少突胶质细胞少前体细胞,OPC非常重要,因为我们神经的传递靠的是电子信号,而OPC的主要功能是作为绝缘体形成髓鞘,保护神经元也阻止电子信号短路,所以OPC的损伤减少会导致神经元受损及脑部疾病,广东话中的〝痴线〞非常形象地解释了OPC的重要性。
“痴线”直译为线路黏连在一起的意思,粤语口语中意为“神经病”,在文中这里也可以引申为神经短路,头脑不清。
通常文章做几个实验证明一个点就可以了,但这篇文章偏不,四大门派用不同的方法及物种做了几十个实验,证明了一系列全新的推论,而且像开了挂一样,每个实验都有很理想的结果,可以顺利导入下一个实验~ 简直是too good to be true。如果笔者当初做实验时能遇上这种事,估计目前还在和老鼠打交道。
这篇文章大大小小实验几十个,还用了多种手段和动物,文章中不断的冷静地述说着各种凡尔赛,每个实验的连接处都是我们证明了A接下来我们推论B然后B又被证明了,于是又再推论C,然后又被证明,不断延长。我都怀疑实验人员是拿了攻略来做实验。
实验一开始还是比较基础的,基本是观察性质。实验人员在少突胶质细胞少前体细胞(OPC)和少突胶质细胞(OL)中发现SIRT2的表达量是最多的(mRNA可以反映基因的表达量)。
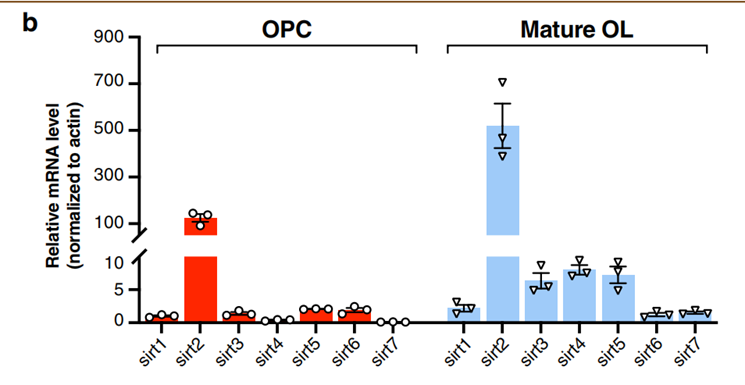
随后实验人员分析SIRT2在大脑皮层的主要细胞中表达量,发现SIRT2主要存在于OPC和成熟的OL,这很可能意味着SIRT2对这两种细胞有作用。
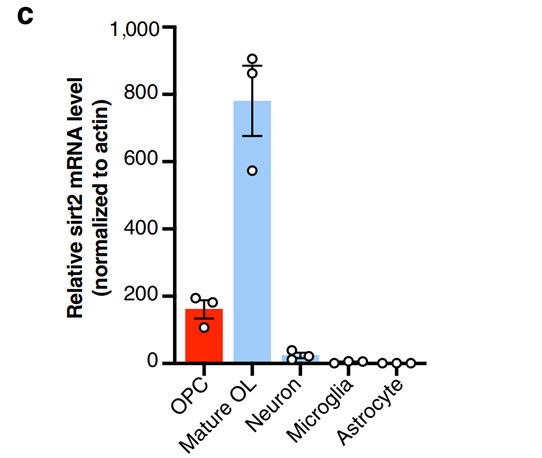
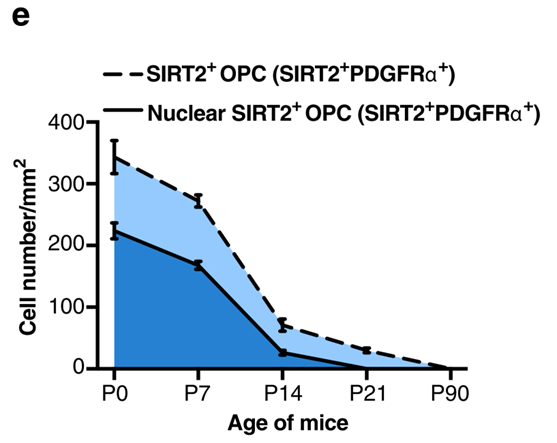
我们知道鼠脑的中枢神经在出生后的21天都是发育异化的关键时间,科学家们发现果然SIRT2在刚出生的头几天的数量最高,到21天至90天已经基本没了。
科学家同时追踪SIRT2在细胞核的数量,发现在头21天中2/3的SIRT2其实是在细胞核中,在21天后,细胞核已经完全没有SIRT2的踪影了,而这一点却是整个文章的关键点!这意味着,SIRT2在OPC的发育中起作用是必须在细胞核中实现,这才有了文章标题中的〞SIRT2重新入核〞。
接着实验丧心病狂的表演出现了,他们不满足于仅仅在实验鼠中验测SIRT2在OPC不同生长阶段的表达,更同时对猴子和人类进行了验测,结果非常正面:SIRT2在不同物种的OPC表达中呈现高度一致性,都是在初期集中在细胞核,在成熟后就只存在于细胞质。也表示SIRT2在脑神经的表达是进化遗传上高度保守,这往往意味着该机制十分重要,只要稍有变异,便会导致没有后代留传下来。

接着,实验还顺便检测了SIRT2在脑部的于年轻和年老时的整体水平,结果也合乎预期,SIRT2在脑部的水平会随衰老而下降,进一步显示SIRT对脑部健康十分重要。
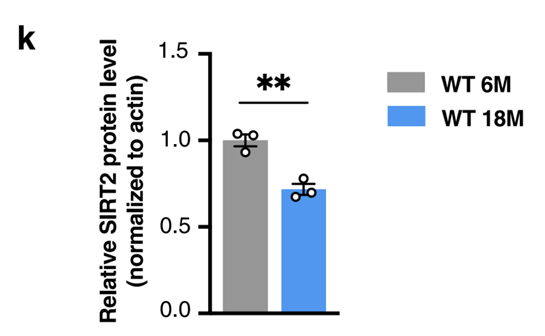
又接着,实验开始由被动观察进入主动干预了。实验鼠被注入溶血卵磷脂(lysolecithin)以促发OPC细胞去髓鞘化,结果发现保护机制起作用,OPC细胞再髓鞘化出现并且和SIRT2表达水平正相关。SIRT2在接受注射的年轻(L-Young) 和年老(L-Old)的实验鼠都出现提升(M,N),只是年轻实验鼠的提升幅度要大于年老实验鼠,而这个差别在细胞核就更明显,年老组只有年轻组的1/3水平(O)。

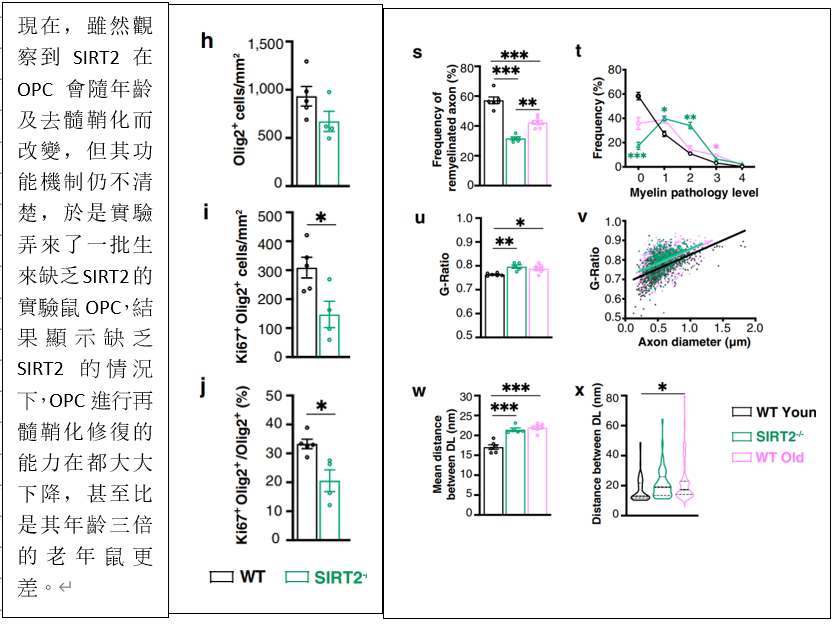
结果表明,SIRT2对OPC的再髓鞘化有着关键的作用。
接着实验人员又引入了另一组基因修改过的实验鼠(G3-Terc-/-)简称G3T,G3T是由于端粒体缺陷而出现早衰的实验鼠。接着实验组发现在实验鼠脑部中NAD+的含量在衰老时会大幅减少,无论是自然衰老还是G3T这样因为基因缺陷而出现的衰老。至此本文章另一重要的玩家NAD+入场了,那NMN还会远吗?
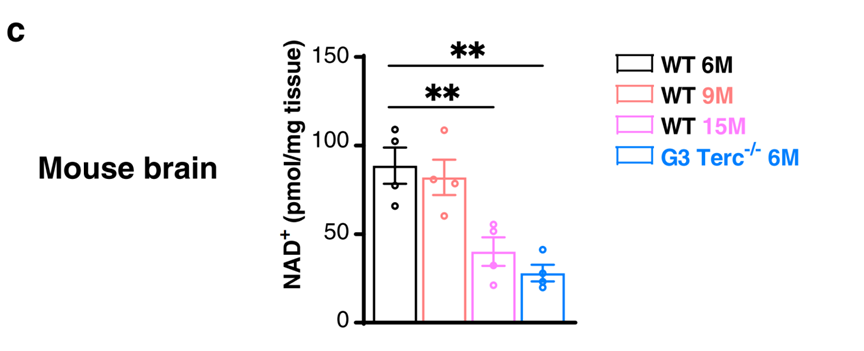
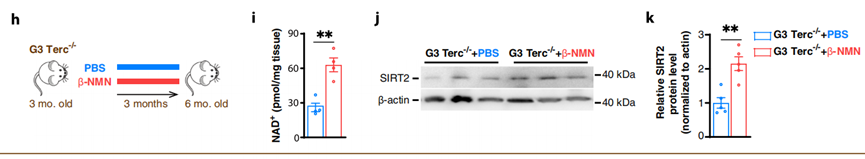
不会的,NMN来了!实验组不出意料的使用了NMN为治疗手段希望看看NMN能否对衰老的实验鼠产生作用,对出现早衰的G3T连续三个月注射NMN后结果完美:
1、三个月后,早衰的G3T脑部NAD+水平大幅提升!(I)
2、三个月后,早衰的G3T脑部SIRT2水平大幅提升!(K)
3、三个月后,受伤的G3T脑部SIRT2在细胞核水平大幅提升!(N)
简直可以说是“神药”级的表现~

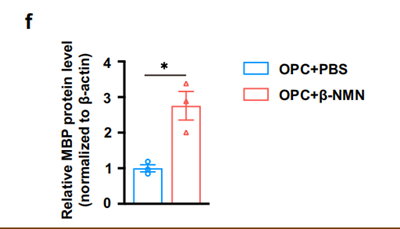
老实说,到这里已经是一篇不错的文章了,但是,为什么不一口吃成个胖子呢?实验决定把NMN提升NAD+的具体功效作为重点研究对象,结果发现NMN能在培养液中大幅提升髓鞘基础蛋白(MBP)。
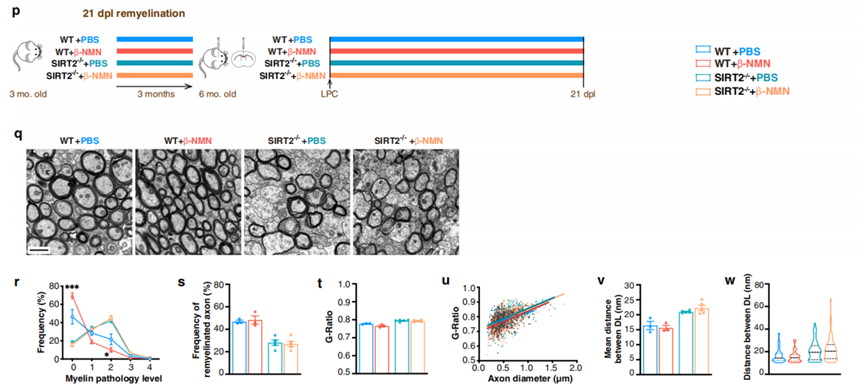
但这只是培养液,不够权威,那在活体呢?实验组在不让人失望上确实没让我失望。这次实验组找了年轻鼠、老年鼠和早衰鼠来做对比,在长期注射NMN(三个月)后,无论是老年鼠还是早衰鼠所有OPC的指标都恢复成和年轻鼠一样!
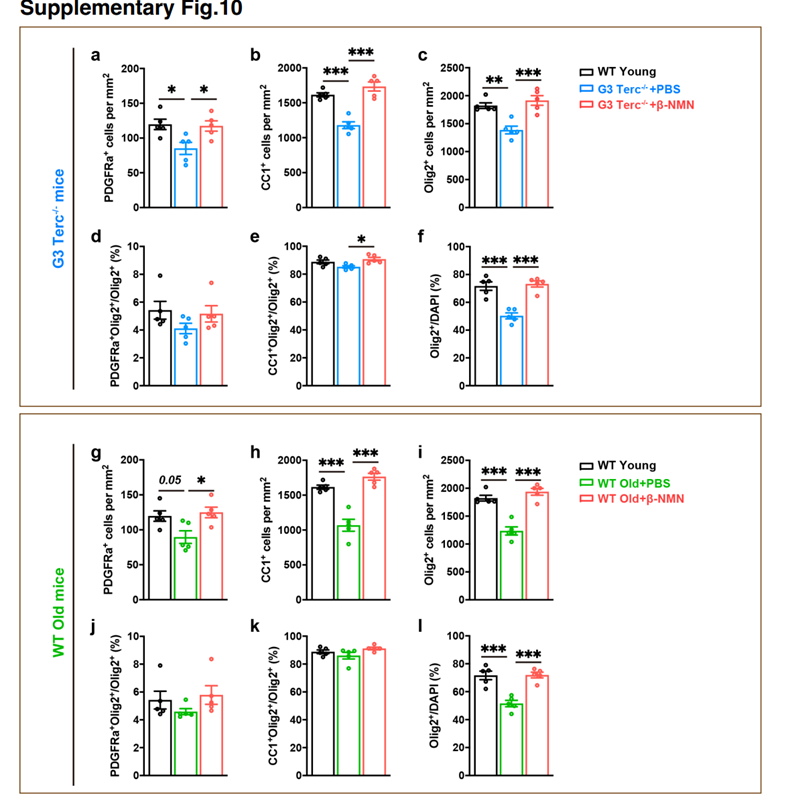
实验组接着比较NMN对髓鞘老化的功效,在长期注射NMN(三个月)后的早衰鼠和老年鼠的脑部各指标都得到改善!尤其明显的是髓鞘病变级别大幅改善,无病变率由20%提升到60%!髓鞘明显加厚!这都表明了,长期补充NAD+能推迟髓鞘老化。

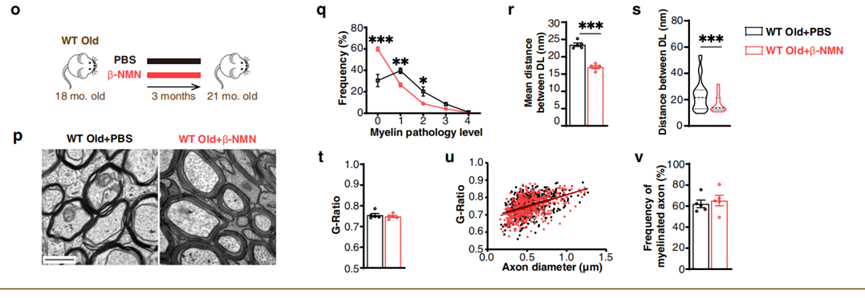
到了这里,我们已经知道,长期补充NAD+能推迟髓鞘老化,这是被动防御,那么,NMN能否修复受伤的髓鞘? 对于开了无敌模式的实验组来说,答案自然是可以。结果表明,在受伤21天后,有注射NMN的早衰鼠再髓鞘化的比例比没有高一倍(M),病变比例也大幅改善(N),神经髓鞘结构也徥到改善(L)。
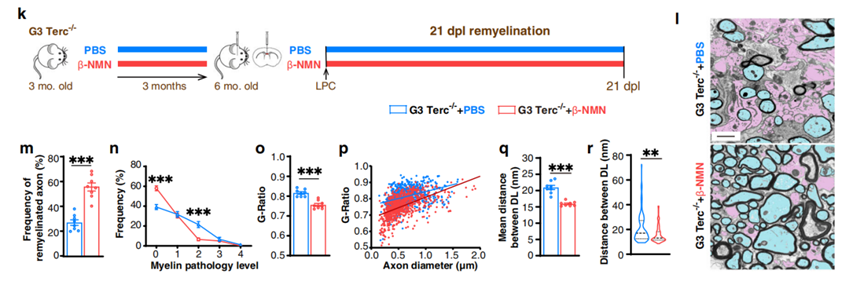
不过这还没完,为了避免扛精挑战进一步证明这些表观的改善在实际的神经传递也同样有效,实验组再做了一件挑战难度的事。实验组拿了实验鼠现切的脑切片去进行神经传递的实验。结果一如所料——完美。
NMN补充剂令早衰鼠受伤21天后的神经传递有效性由等同年轻鼠的40%提升到92%(V),更令人信服的是,这些改善后的神经传递的快慢模式和年轻鼠也没有分别(X,Y)。
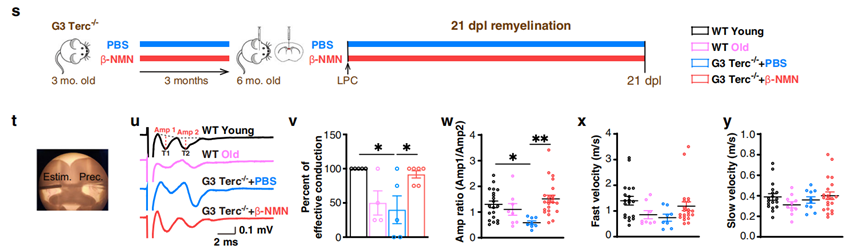
实验到这里,已经相当完美的显示出NMN对预防及修复脑部细胞的功效。但是只有结果没有理论的文章不是完美的文章,于是实验组开始对NMN及SIRT2关系左右横跳进行测试:
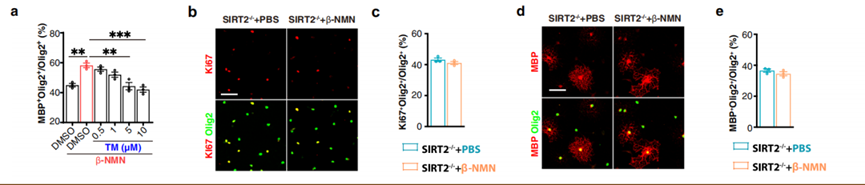
实验一,实验组在培液中加入SIRT2的抑制剂(TM),结果发现TM浓度加到一定种度,NMN对OPC的保护作用消失(A)。
实验二,有SIRT2缺陷的小鼠细胞中,OPC发育加不加NMN的结果一样。
实验X,有SIRT2缺陷的小鼠细胞中,受伤后加不加NMN的结果一样。
因此证明了NMN必须要配合SIRT2才能发挥对OPC的保护及修复作用。
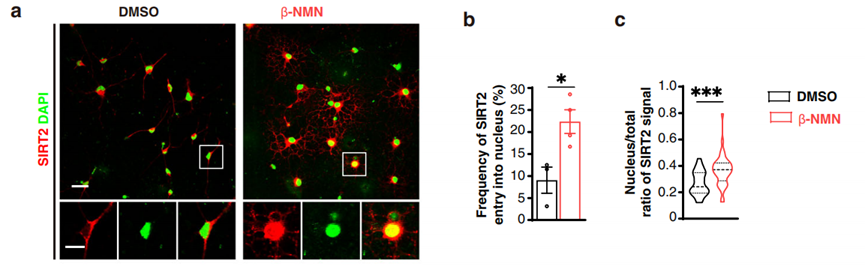
接着,实验又发现NMN能够促进SIRT2重新进入细胞核。
再然后,实验又把瞄头对准了体内的另一个影响到OPC功能的分子-ID4,ID4是OPC的抑制剂,ID4在早衰鼠和SIRT2缺陷的体内会大量出现,导致OPC功能受限。
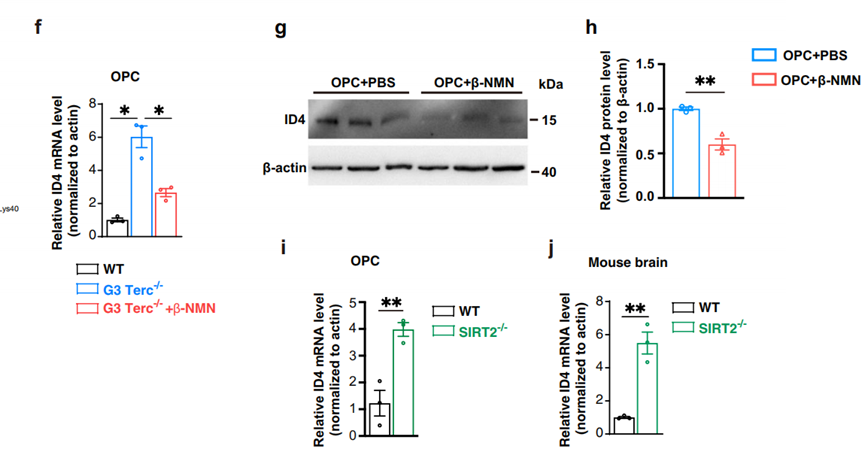
实验接着尝试找出SIRT2和ID4之间互动的情况,发现SIRT2会通过直接粘附于ID4的启动因子(L)及去乙酰化H3K18AC(M)来实现抑制ID4的活性从而保护OPC。
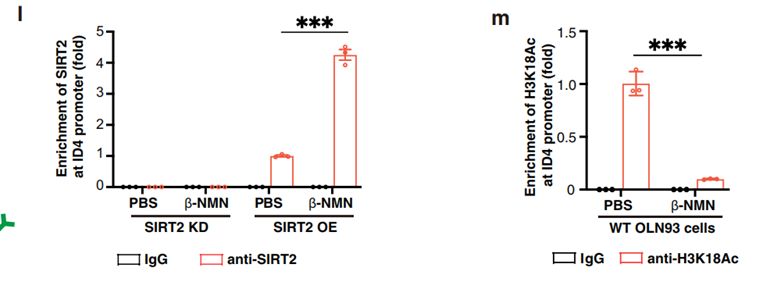
最后,把文章升华的地方就是提出理论假想:老化的OPC会表现出细胞核SIRT2减少,NAD+较低。而补充NMN可以提高NAD+水平,恢复SIRT2入核并且并使H3K18去乙酰化,从而抑制ID4,达到促进OPC分化发育的效果。补充恢复NAD+水平重现 OPC中SIRT2进入细胞核,促进OPC分化成成熟的少突胶质细胞,并最终推迟正常中枢神经系统中髓鞘老化,增强髓鞘在脱髓鞘老化的中枢神经系统修复。
因为文章太长太详细,最后这里把概述和总结简单说下:
在大脑的中枢神经系统(CNS)需要以由少突胶质细胞(OL)组成的髓鞘(myelin)包裹缠绕神经元的轴突以实现神经信号的正确传递。但是髓鞘会出现老化或受损,从而引起起的髓鞘病变及脱离,称为去髓鞘(demyelination),这也是我们CNS衰老的重要原因。在我们年轻时,去髓鞘可以通过少突胶质细胞前体细胞(OPC)分化发育为新的成熟的OL,形成新的髓鞘包裹轴突,实现髓鞘的再生(remyelination)。
而大脑的中枢神经系统(CNS)老化的原因之一正是因为OPC老化令分化发育的能力下降导致髓鞘的再生和修复能力下降。因此,这次文章就在寻找重新年轻化OPC的方法。
实验组通过在早衰鼠、SIRT2缺陷鼠和老鼠配合多种研究手段,终于发现了:
1、SIRT2 对小鼠的OPC和OL生至关重要,而且SIRT2 在 OPC发育初期需要进入细胞核。而且这套机制遗传学上高度保守,在鼠、猴和人身上基本一致。
2、通过补充NMN可以实现NAD +提高、SIRT2提高及SIRT2入核。
3、通过补充NMN可以推迟体内老年小鼠的髓鞘老化可增强体内老年小鼠的髓鞘再生修复。
4、NMN对髓鞘再生的增强作用需要 SIRT2。
最后,令文章提升到自然杂志级别的机制推论:NMN 提升NAD+促使 SIRT2 进入细胞核,SIRT2在核内令H3K18去脱乙酰从而抑制 ID4 转录,促进MBP的转录,实现 OPC 重拾活力,最终推迟髓鞘的老化,促进老年髓鞘的损伤修复。
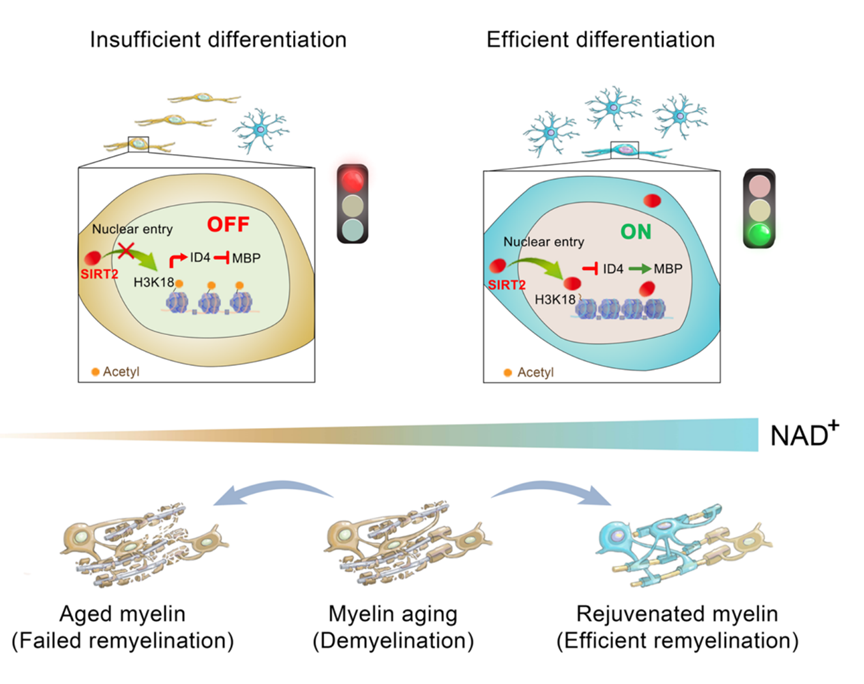
这论文的实际意义在于揭示了补充β-NMN可以推迟髓鞘老化并促进髓鞘损伤后的修复。NMN确实有可能成为预防中枢神经系统髓鞘老化和脱髓鞘疾病治疗的新的分子靶点和候选药物。